量子化学分科
関連リンク:量子化学研究室のホームページ
振動分光法によりタンパク質でおこる化学反応を理解する
タンパク質では「構造変化」という化学反応をともなって、機能が生み出されます。タンパク質分子にはスイッチとして働く部位と、機能を生み出すために働く部位があります。外部からの刺激のセンサーとなるスイッチ部位において局所的だった構造変化は、部位間で連動しながら、時間が経つにつれてタンパク質分子全体へと広がります。連動して起こる構造変化を、変化の途中で順を追ってとらえることができれば、タンパク質分子が機能する仕組みを明らかにすることができます。このためには、原子レベルでの空間分解能および反応の過程を追跡できる時間分解能を持った観測、かつ反応全体をカバーした観測が必要です。
原子レベルでの分子構造変化を観測するためには、X線結晶構造解析や電子顕微鏡を用いて原子位置座標を明らかにする方法が広く用いられています。これに対して本研究グループでは、振動分光法であるラマン分光法を用いて、化学結合の変化に着目した研究を行っています。ラマン散乱における共鳴効果を利用することで、タンパク質中の特定の部位での構造変化を選択的に観測することができます。さらに、時間分解分光法を組み合わせることにより、分子構造が時々刻々と変化するプロセスを追跡することができます。機能のスイッチングに光化学反応を用いる時間分解共鳴ラマン分光計測により、タンパク質の構造ダイナミクスと機能の相関を調べ、タンパク質分子の仕組みを明らかにします。
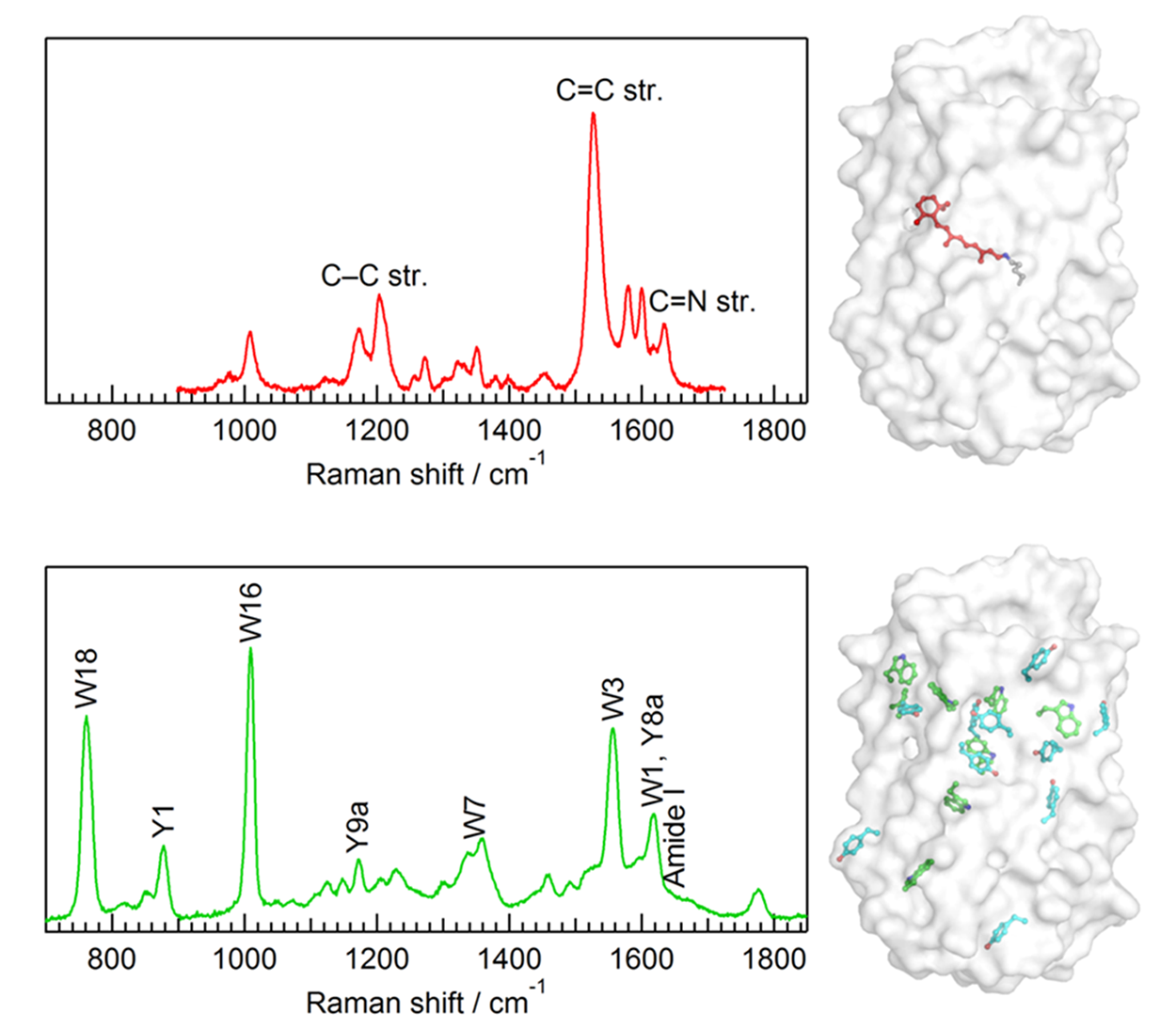
レチナールタンパク質の共鳴ラマンスペクトル.
(上)可視光(~500 nm)によりラマン散乱を励起:可視光領域に電子吸収をもつレチナール発色団のラマンバンドが選択的に観測できる.
(下)紫外光(~230 nm)によりラマン散乱を励起:紫外光領域に電子吸収を持つ芳香族アミノ酸であるトリプトファン(W)やチロシン(Y)に由来するラマンバンド、ポリペプチド鎖に由来するアミド振動のラマンバンドが選択的に観測できる.
タンパク質の仕組みを利用する
タンパク質中のヘムは、可視光を吸収すると、高速な無輻射緩和により入力した光エネルギーを効率よく熱エネルギーに変換します。ラマン分光法を用いたこれまでの実験研究により、タンパク質中の光励起したヘムを熱源としたエネルギーフローを観測し、タンパク質分子における熱拡散の仕組みが明らかになりました。この結果から、ヘムタンパク質が光熱エネルギー変換分子ヒーターとしての優れたポテンシャルを持つことが示されました。
実験により知りえたタンパク質分子の仕組みを利用して、光スイッチングによる熱シグナル制御を行い、細胞を操る技術開発を行います。これにより、物理化学と生命科学の架け橋となる研究を目指します。
光熱エネルギー変換タンパク質ヒーター
(最終更新日:2024年04月04日)
